我院成功举办“药物及医疗器械试验质量管理规范”学习班
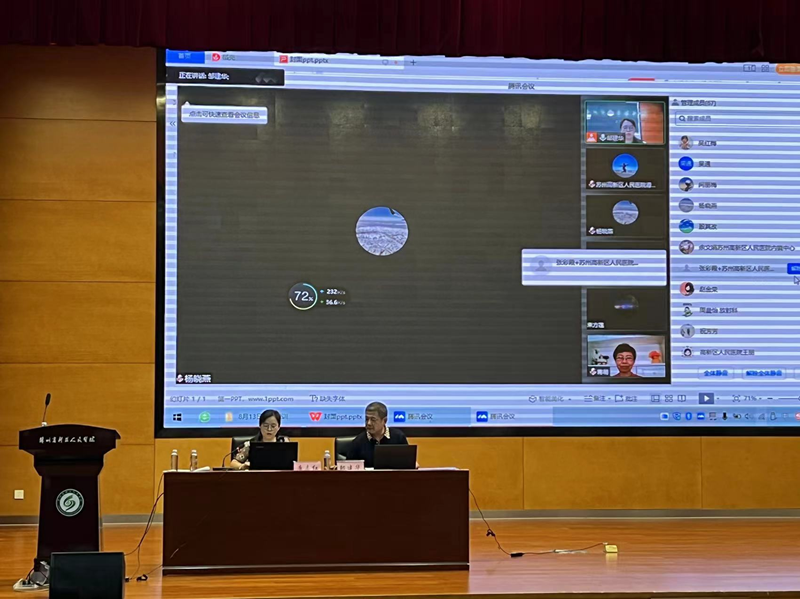
为积极创建国家药物临床试验机构,促进医疗机构临床药物试验顺利进行,8月13日,我院与南京药学会于联合举办“药物及医疗器械临床试验质量管理规范”学习班,会议采取线上线下同步进行的模式。院长(机构主任)梅冰、机构办公室人员、伦理委员办公室人员、三个申报专业组成员及其他临床科室骨干等共150余人参加了会议。
江苏省中医院蒋萌教授、南京医科大学第一附属医院李天萍主任、东南大学附属中大医院王慧萍主任、南京医科大学附属逸夫医院苏钰文主任、南京医科大学第二附属医院张会杰主任、南京医科大学第一附属医院张馥敏主任等6位专家围绕着药物临床试验中不同角色研究者的职责、新版《药物临床试验质量管理规范》解读、新机构的建设与管理、临床试验中的安全性事件管理、新版《医疗器械临床试验质量管理规范》解读、新版GCP中伦理审查要求与受试者保护六大主题进行了全面、细致的讲解,对我院新机构的备案工作有着至关重要的作用。
本次学习班由机构办公室主任邹建华主持,会议开始,南京药物临床试验专委会主任委员蒋萌教授与我院副院长(机构副主任)唐志红进行致辞。会上唐院强调了成立药物临床试验机构对我院发展的重要意义,指出医院高度重视临床科研工作,申报药物临床试验机构,获得药物临床临床试验机构资格,有助于加强我院同高水平科研机构的交流协作,增强学科建设能力,进而提升医院的综合实力,为医院创建三级医院做好铺垫。
本次学习班对我院研究者掌握新版GCP很有帮助,使研究者们更加清晰地了解开展临床试验工作需关注的重点,以不断提升药物及医疗器械工作水平,为后期规范开展临床试验打好基础。
会议结束,针对当日学习内容,全员参加线下理论考核,考试合格者后方可获得GCP培训证书。学习班的举办,使大家对临床试验各方面的认知得到了提高,能够极大的提高医院的临床科研水平,进一步推动我院科研工作的发展。
药剂科:雷琼
审核:邹建华